Índice
Qué es el SIBO: planteamiento
El sobrecrecimiento bacteriano del intestino delgado (SIBO) es un exceso de bacterias en el intestino delgado y una enfermedad poco conocida. Al principio se creía que ocurría en solo un pequeño número de pacientes, pero ahora es evidente que este trastorno es más prevalente de lo que se pensaba.
El crecimiento excesivo de bacterias provoca síntomas gastrointestinales. Los pacientes con SIBO varían en la sintomatología, desde ser levemente sintomáticos hasta sufrir diarrea crónica, pérdida de peso y malabsorción. Actualmente se dispone de una serie de pruebas de diagnóstico, aunque el régimen de tratamiento óptimo sigue siendo difícil de alcanzar.
Es especialmente relevante que existe un interés en el SIBO y su supuesta asociación con el síndrome del intestino irritable. A continuación abordamos un poco de la epidemiología, patogénesis, manifestaciones clínicas, el diagnóstico y tratamiento del SIBO.
El aparente aumento en la prevalencia del SIBO puede haber ocurrido, en parte, porque las pruebas de diagnóstico fácilmente disponibles han mejorado nuestra capacidad para diagnosticar SIBO.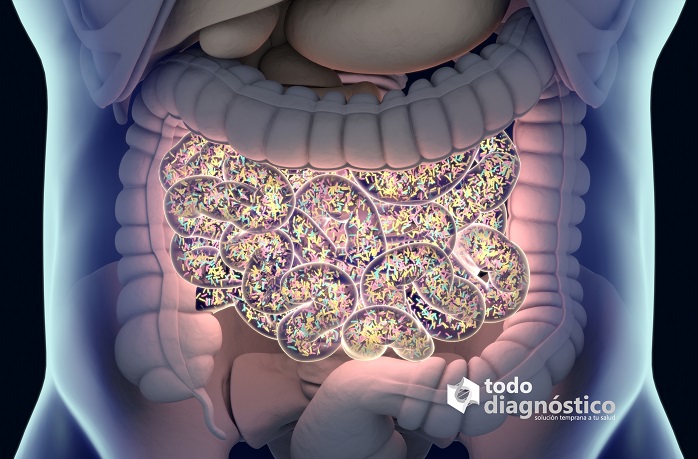
Definición
SIBO se define como una población bacteriana en el intestino delgado que excede los 105-106 organismos por ML. Por lo general se encuentran menos de 103 organismos / mL en la parte superior del intestino delgado, y la mayoría de estos son bacterias grampositivas.
Además del número absoluto de organismos, el tipo de flora microbiana presente juega un papel importante en la manifestación de signos y síntomas de sobrecrecimiento. Por ejemplo, un predominio de bacterias que metabolizan las sales biliares a compuestos no conjugados o insolubles puede conducir a la formación de grasa, malabsorción o diarrea de ácidos biliares. Por otro lado, los microorganismos que metabolizan preferentemente los carbohidratos a ácidos grasos de cadena corta y gas pueden producir hinchazón sin diarrea porque los productos metabólicos pueden absorberse.
Los coliformes gramnegativos como las especies de Klebsiella, pueden producir toxinas que dañan la mucosa. Esto interfiere con la función de absorción y causa secreción, imitando así el esprúe tropical.
Prevalencia
Solo se dispone de datos limitados sobre la prevalencia de SIBO en poblaciones sanas. Sin embargo, las tasas de prevalencia de SIBO en adultos jóvenes y de mediana edad parecen ser bajas, mientras que la prevalencia las pruebas parecen ser consistentemente más altas en los pacientes mayores. Es especialmente relevante mencionar que estos resultados dependen de la prueba de diagnóstico utilizada.
Patogénesis
SIBO se desarrolla cuando se alteran los mecanismos homeostáticos normales que controlan las poblaciones de bacterias entéricas. Los dos procesos que predisponen con mayor frecuencia al crecimiento excesivo de bacterias son la secreción disminuida de ácido gástrico y la dismotilidad del intestino delgado.
Otros factores que aumentan la probabilidad de desarrollar SIBO son las alteraciones en la función inmunológica intestinal y las anomalías anatómicas del tracto gastrointestinal. Una vez presente, el sobrecrecimiento bacteriano puede inducir una respuesta inflamatoria en la mucosa intestinal, exacerbando aún más los síntomas típicos de SIBO. Aunque no se observa de forma universal, el sobrecrecimiento bacteriano en la flora intestinal del intestino delgado puede provocar una inflamación microscópica de la mucosa. El análisis de biopsias de intestino delgado en adultos mayores con crecimiento bacteriano excesivo reveló embotamiento de las vellosidades intestinales. También un adelgazamiento de la mucosa y criptas, y un aumento de linfocitos intraepiteliales, todo lo cual se revirtió con tratamiento antibiótico.
Desde finales de la década de 1990 ha habido un resurgimiento en la investigación de SIBO gracias al conocimiento cada vez mayor del microbioma intestinal y sus funciones en la salud y el desarrollo de enfermedades. Estos incluyen una serie de artículos que relacionan SIBO con enfermedades como el síndrome del intestino irritable, la enfermedad inflamatoria intestinal, esclerosis sistémica, trastornos de la motilidad, cirrosis, hígado graso y una variedad de otras afecciones.
Ácido gástrico
El ácido gástrico suprime el crecimiento de las bacterias ingeridas, lo que limita el recuento de bacterias en la parte superior del intestino delgado. La disminución de la producción de ácido (hipoclorhidria) es un factor de riesgo de SIBO. Esto puede desarrollarse después de la colonización por Helicobacter pylori o como consecuencia del envejecimiento.
El crecimiento excesivo de bacterias puede conducir a un falso positivo en el diagnóstico de Helicobacter pylori mediante pruebas basadas en urea dada la presencia de cepas bacterianas ureasa positivas. La inhibición de la secreción de ácido a través de bloqueadores del receptor de histamina tipo 2 (H2RA) o inhibidores de la bomba de protones (IBP) puede predisponer a SIBO, aunque se encuentran resultados contradictorios en la literatura disponible.
Trastornos de la motilidad
La motilidad gastrointestinal normal implica una serie compleja y estrechamente coordinada de eventos diseñados para mover material a través del tracto gastrointestinal. Durante los periodos de ayuno, se desarrolla un complejo motor migratorio aproximadamente cada 90 a 120 minutos para barrer los desechos residuales. Varios estudios han demostrado que las anomalías en los complejos motores migratorios pueden predisponer al desarrollo de SIBO. La peristalsis posprandial incluye contracciones irregulares de gran amplitud en el estómago (para ayudar con la trituración y el vaciamiento gástrico). Mientras tanto, la gastroparesia es un trastorno crónico de retraso vaciamiento gástrico. Por lo general se desarrolla como consecuencia de una diabetes de larga duración, trastornos del tejido conectivo, una infección viral previa o isquemia. La alteración de la peristalsis gástrica puede provocar SIBO debido a la estasis de alimentos y a bacterias del tracto gastrointestinal superior.
Los trastornos de la motilidad del intestino delgado también predisponen al desarrollo de SIBO porque las bacterias pueden no ser barridas de manera efectiva desde el intestino proximal hacia el colon. Asimismo, los pacientes con insuficiencia renal crónica tienen anomalías motoras de tipo neuropático en el intestino delgado y es más probable que desarrollen sobrecrecimiento bacteriano.
Anomalías estructurales del tracto gastrointestinal
Una anomalía estructural en el tracto gastrointestinal proporciona un entorno ideal para el sobrecrecimiento bacteriano. Las cirugías del tracto gastrointestinal que crean un bucle ciego (como una gastrectomía Billroth II o una anastomosis en Y de Roux) predisponen a la estasis bacteriana y al crecimiento excesivo debido a la motilidad anormal y la eliminación ineficaz de los alimentos retenidos y secreciones.
Los pacientes que se han sometido a una derivación yeyunoileal, una anastomosis enteroentérica terminolateral o la creación de una bolsa ileal distal de Koch también corren el riesgo de desarrollar SIBO.
Es especialmente relevante que los divertículos del intestino delgado ocurren en aproximadamente uno a 6% de la población, según estudios de autopsias y una variedad de estudios radiográficos. Por lo general, son incidentales, asintomáticos y de tamaño pequeño. No obstante, los divertículos duodenales y yeyunales grandes pueden albergar bacterias y provocar síntomas de SIBO.
Las estenosis del intestino delgado puede desarrollarse después de una cirugía, radiación, en asociación con la enfermedad de Crohn, o debido al uso de medicamentos, lo cual también predispone al sobrecrecimiento de bacterias.
Función inmune
Los pacientes inmunodeprimidos, ya sea debido a una respuesta anormal de anticuerpos o de células T, son propensos al crecimiento excesivo de bacterias. La evidencia disponible sugiere que los pacientes con SIBO (en comparación con aquellos con aspirados yeyunales normales) tenían más probabilidades de tener anomalías en la inmunidad de la mucosa intestinal (evidenciado por aumento de las concentraciones de inmunoglobulina A [IgA] luminal y recuentos de células plasmáticas de IgA de la lámina propia). Los pacientes con deficiencias en la inmunidad humoral o celular no parecen estar predispuestos a SIBO, ya que tienen una microflora intestinal normal.
Manifestaciones clínicas
Los síntomas de SIBO son inespecíficos e incluyen hinchazón, distensión abdominal, dolor o malestar abdominal, diarrea, fatiga y debilidad. La frecuencia y la gravedad de los síntomas probablemente reflejen tanto el grado de sobrecrecimiento bacteriano como el grado de inflamación de la mucosa. Sin embargo, los síntomas también pueden reflejar la causa subyacente de SIBO. Por ejemplo, dismotilidad del intestino delgado. Otros síntomas como la malabsorción, deficiencias nutricionales y trastornos óseos metabólicos pueden reflejar complicaciones de SIBO.
La naturaleza inespecífica de las manifestaciones clínicas hace que SIBO sea difícil de distinguir clínicamente de otras enfermedades, como el ya mencionado síndrome del intestino irritable, además de la intolerancia a la lactosa o fructosa. Ningún estudio ha evaluado la especificidad de estos síntomas, por lo que se recomienda realizar pruebas objetivas.
Complicaciones
Las complicaciones de SIBO varían desde leves, que incluyen diarrea y deficiencias mínimas de vitaminas, hasta graves, que incluyen malabsorción y neuropatías debido a deficiencias de vitaminas liposolubles. Las consecuencias nutricionales del SIBO son el resultado de una mala digestión y malabsorción de nutrientes en la luz intestinal. Esto último ocurre como consecuencia del daño microscópico de la mucosa del intestino delgado que disminuye la capacidad de absorción de las microvellosidades.
Diagnóstico
Existe un desacuerdo sustancial en la literatura sobre qué prueba es la más apropiada en el ámbito clínico o de investigación para el diagnóstico de SIBO. Normalmente se emplean dos pruebas: cultivo bacteriano y pruebas de aliento.
Los desafíos de medir directamente la contaminación bacteriana del intestino delgado llevaron al desarrollo de varias pruebas indirectas para el diagnóstico de SIBO. Las pruebas de aliento son ahora el método predominante para evaluar a los pacientes en busca de un posible crecimiento excesivo. Eso se debe a su simplicidad, seguridad y a que no son invasivas. Todos estos métodos se basan en la modificación de un sustrato por bacterias. El sustrato más comúnmente utilizado es un carbohidrato que se metaboliza fácilmente, como lactulosa, glucosa, sacarosa o xilosa. Los carbohidratos complejos, como el arroz, no son sensibles ni específicos.
Dado que la definición clínica de SIBO no es clara en ausencia de resultados validados informados por el paciente, el uso de pruebas de aliento para el diagnóstico de SIBO se reconoce como un aspecto clave.
Prueba de aliento
La medición cuantitativa de hidrógeno o metano en el aliento es una prueba relativamente económica, no invasiva, fácil y ampliamente disponible. Los kits de pruebas de aliento más nuevos están disponibles para pruebas en el hogar para pacientes que no pueden viajar o están en lugares remotos. A menudo, estos kits están dirigidos a laboratorios con certificación de enmiendas de mejora y como tal, tienen una supervisión de validación y calibración estricta, en comparación con los consultorios médicos privados. Sin embargo, las precauciones dietéticas antes de la prueba, la ingestión de sustrato y la recolección de la prueba de aliento se realizan en un entorno doméstico que puede no estar estrictamente controlado.
La premisa de las pruebas de aliento es que las células humanas son incapaces de producir hidrógeno y gases metano. Por lo tanto, si estos gases pueden detectarse en muestras de aliento, significa que provienen de otra fuente. Por ejemplo, de la fermentación de carbohidratos por microbios en el intestino, su posterior absorción en el torrente sanguíneo y su expiración a través de los pulmones.
Después de la ingestión de una carga de carbohidratos y su exposición a bacterias, el azúcar se fermenta rápidamente para producir gas hidrógeno junto con ácidos grasos de cadena corta. En pocas palabras, el aumento en las concentraciones de hidrógeno en las muestras de aliento facilita el diagnóstico de SIBO.
Antes de la prueba de aliento se recomienda que los pacientes eviten el uso de antibióticos durante cuatro semanas. También se sugiere evitar los agentes promotores y laxantes durante al menos una semana. El día antes de la prueba de aliento debe evitarse los alimentos fermentables y los pacientes deben ayunar durante ocho a 12 horas. Finalmente, durante la prueba de aliento, los pacientes deben evitar fumar y minimizar el esfuerzo físico.
Aspirado y cultivo de intestino delgado
El aspirado y el cultivo del intestino delgado a menudo se consideran el estándar de oro para el diagnóstico de SIBO. Para la recolección aséptica de muestras de aspirado del intestino delgado faltan técnicas estandarizadas. Esto se debe a que los métodos difieren en cuanto a la ubicación del dispositivo para el aspirado y la cantidad de líquido recolectado, así como el manejo de la muestra y el cultivo posterior.
En general, durante una endoscopia superior, se puede lograr una intubación duodenal profunda mientras se minimiza la succión durante la inserción del endoscopio a través de la boca y el estómago. Con esto se evita la contaminación cruzada de las secreciones del exterior del duodeno. En una técnica, se pasa un catéter con múltiples orificios laterales a través del canal de biopsia de un endoscopio superior hacia la tercera y cuarta porciones del duodeno. Con una succión suave, se aspira aproximadamente tres a cinco ML de líquido duodenal y la muestra se envía a un laboratorio de microbiología para su cultivo.
El uso de guantes estériles tanto por parte del endoscopista como del asistente al ensamblar el catéter y recolectar muestras y colocar un tapón estéril en la jeringa son todos componentes clave para la recolección y manipulación adecuadas de las muestras. Una vez obtenida, la muestra debe transferirse de inmediato a un laboratorio de microbiología con procesamiento rápido para cultivos aeróbicos y anaeróbicos. Es importante comunicarse con el personal del laboratorio con respecto al uso de medios apropiados. Finalmente, en lugar de informar los resultados como positivos o negativos es necesario describir el crecimiento de organismos como un recuento de colonias preciso en UFC / mL.
Fuentes de consulta:
Andrew C. Dukowicz, et.al.. (2007). Small Intestinal Bacterial Overgrowth. 15 de abril de 2021, de Gastroenterology & Hepatology Sitio web: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3099351/
Pimentel, Mark. et.al.. (2020). ACG Clinical Guideline: Small Intestinal Bacterial Overgrowth. 15 de abril de 2021, de The American Journal of Gastroenterology Sitio web: https://journals.lww.com/ajg/fulltext/2020/02000/acg_clinical_guideline__small_intestinal_bacterial.9.aspx